입력 2026.03.20 10:39
- CRISPR-Cas9 억제하는 새로운 항-크리스퍼 기전 발견
- 기존 단백질 표적 방식과 달리 RNA를 직접 겨냥하는 혁신적 메커니즘 제시
- 유전자 편집 기술의 정밀 제어 및 안전성 향상 기대

중앙대학교 (총장 박세현) 연구진이 유전자 가위 기술로 널리 활용되는 CRISPR-Cas9 시스템을 억제하는 완전히 새로운 방식의 항-크리스퍼 (anti-CRISPR) 작용 기전을 세계 최초로 규명했다. 중앙대 약학대학 박현호 교수 연구팀은 항-크리스퍼 단백질 중 하나인 AcrIIA7을 동정하고 그것의 구조와 기능을 정밀 분석하여, 이 단백질이 기존과는 전혀 다른 방식으로 CRISPR-Cas9을 억제한다는 사실을 규명했다고 밝혔다.
이번 연구는 한국연구재단이 주관하는 바이오의료기술개발 사업의 지원을 받아 수행되었으며, 연구 결과는 생명과학 분야의 권위 있는 국제 학술지 Nature Communications (Impact Factor 15.7) 에 ‘AcrIIA7은 CRISPR-Cas 시스템을 저해하기 위해 tracrRNA를 납치한다 (AcrIIA7 hijacks tracrRNA to block CRISPR-Cas system)’ 라는 제목으로 게재됐다.
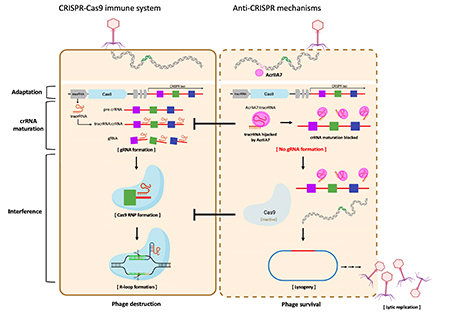
CRISPR-Cas9 시스템은 외부 침입자의 DNA를 인식하고 절단하는 박테리아의 면역 시스템으로, 특정 서열의 DNA를 자르는 특성상 유전자 치료 및 생명공학 분야에서 핵심 기술로 활용되고 있다. 이 시스템은 Cas9 단백질과 함께 crRNA와 tracrRNA가 결합된 복합체 (RNP) 가 형성되어 활성화 된다. 연구팀은 AcrIIA7이 기존 항-크리스퍼 단백질들과 달리 Cas9 단백질에 직접 결합하지 않고, 대신 tracrRNA에 특이적으로 결합하여 기능을 억제한다는 사실을 밝혀냈다. 이 과정에서 AcrIIA7이 tracrRNA를 hijacking하여 crRNA와의 결합을 방해하고, 결과적으로 Cas9 활성에 필수적인 RNP 복합체 형성을 차단함을 확인했다. 이런 현상을 기반으로 기존에 알려진 항-크리스퍼 작용과는 완전히 다른, RNA 기반 억제 메커니즘을 제시하였다.
연구팀은 X-ray 결정학과 생화학적 분석을 통해 AcrIIA7의 3차 구조를 규명하고 이 단백질이 4량체 형태로 존재하며 RNA결합에 적합한 양전하 구조를 형성함을 확인하였다. 특히 AcrIIA7의 특정 구조 영역이 tracrRNA의 stem-loop 구조를 선택적으로 인식하여 결합하는 것을 밝혀냈으며, 이를 통해 RNA 구조 의존적 인식 메커니즘을 제시했다. 이런 tracrRNA를 AcrIIA7이 납치하여 Cas9의 활성에 결정적인 gRNA형성을 막고 Cas9-RNP 복합체 형성을 저해하는 억제 메커니즘을 규명하여 제시하였다. 이런 방식의 항-크리스퍼의 억제 메커니즘은 기존 단백질 표적 방식에서 벗어나 RNA를 직접 표적으로 하는 제어 전략을 제시했다는 점에서 학문적, 기술적 의미가 매우 크다.
박현호 교수는 “이번 연구는 항-크리스퍼 단백질이 RNA를 직접 표적으로 삼아 CRISPR 시스템을 억제할 수 있다는 새로운 개념을 제시한 것”이라며, “향후 유전자 가위 기술을 보다 정밀하고 안전하게 제어할 수 있는 핵심 원천기술로 활용될 수 있을 것 ”고 말했다.