입력 2026.03.10 14:15
- 유전자형에 따라 아연 결핍 취약성 달라질 수 있어… 정밀영양 전략 단서 제시

빈혈은 영양학적 중재를 통해 예방 및 개선이 가능한 질환 중 세계에서 가장 흔한 질환이다. 특히 철 결핍성 빈혈은 대표적인 공중보건 문제로 꼽힌다. 그러나 빈혈은 단순히 철 결핍만으로 설명되지 않으며, 철 보충이 모든 환자에서 동일한 효과를 보이는 것도 아니다. 최근에는 철 이외의 미량금속과 영양소가 적혈구 생성에 중요한 역할을 한다는 점이 주목받고 있으나, 이들 간 상호작용이 빈혈 위험을 어떻게 조절하는지에 대한 분자적 기전은 충분히 밝혀지지 않았다.
아연은 철과 함께 인체에 필수적인 미량금속이다. 혈중 농도 변동이 작고 항상성 조절이 엄격하게 유지되는 특성상 개인의 아연 영양 상태를 정량적으로 평가할 수 있는 특이적 진단 기법이 아직 확립되어 있지 않다. 이로 인해 임상적으로 아연 결핍을 조기에 진단하기 어렵고, 예방적 접근의 중요성이 더욱 강조되고 있다. 특히 개인의 유전적 배경에 따라 아연 결핍에 대한 민감도가 달라질 수 있다면, 이는 기존의 일률적 영양 권고를 넘어선 새로운 접근을 요구한다.
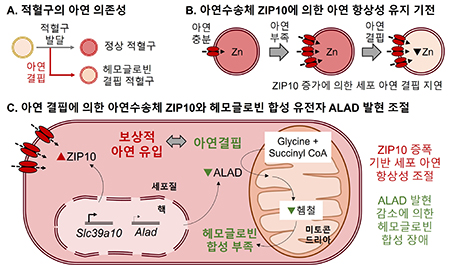
연세대학교 식품영양학과 류문선 교수 주도 아래, 미국 플로리다대학교, 조지아대학교, 네브라스카대학교 연구진이 참여한 글로벌 협력 연구팀은 아연 수송체 ZIP10(유전자명: SLC39A10)이 아연 결핍 상황에서 적혈구 내 아연 항상성을 유지하고 헴철(heme iron) 합성을 보호하는 핵심 조절 인자임을 규명했다. 특히 ZIP10 기능이 저하되거나 해당 유전자에 변이가 존재할 경우, 세포 내 아연 균형이 쉽게 무너지고 헴철 합성이 감소해 빈혈 위험이 높아질 수 있음을 분자·세포 수준에서 검증했다. 해당 연구 성과는 세계적 권위의 학술지 Proceedings of the National Academy of Sciences(PNAS)에 게재됐다.
연구팀은 오믹스 기반 전사체 분석을 통해 아연이 결핍된 환경에서 분화 중인 적혈구 전구세포의 유전자 발현 변화를 정밀 분석했다. 그 결과, 헴철 생합성에 필수적인 효소 ALAD의 발현이 선택적으로 억제된다는 사실을 확인했다. 이는 단순한 세포 스트레스 반응이 아니라, 아연 의존적 대사 경로가 특이적으로 교란된 결과임을 보여준다. 즉, 아연 결핍은 헴철 합성 경로의 핵심 단계에서부터 적혈구 생성 효율을 저해할 수 있음을 의미한다. 연구팀은 유전자 기능 저하 조건에서 세포가 아연 결핍에 더욱 민감하게 반응한다는 점을 실험적으로 확인함으로써, 유전자 활성 수준이 아연 결핍 취약성을 결정할 수 있음을 제시했다.
류문선 교수는 “이 연구는 아연이 적혈구 생성 과정에서 헴철 합성을 정밀하게 조절하는 핵심 인자임을 분자 수준에서 규명한 연구”라며 “특정 아연 수송체 유전자 변이를 가진 경우 아연 결핍에 더 취약할 수 있다는 점에서, 유전자 정보를 활용한 위험 예측과 예방 중심의 영양 전략 수립에 중요한 과학적 근거를 제공한다”고 설명했다.
이번 연구는 미량금속 대사라는 기초 영양학적 질문을 오믹스 분석과 인구 유전학 데이터를 통합해, 유전자 변이에 따른 빈혈 위험 예측 가능성을 제시했다. 특히 아연 결핍을 정량적으로 진단하기 어려운 현실에서, 유전자 정보를 기반으로 한 위험도 평가가 새로운 보완 전략이 될 수 있음을 보여준다. 이는 공중보건 영양학과 정밀영양학을 연결하는 대표적 사례로, 향후 유전자형 기반 영양 중재 전략 개발의 학문적 토대가 될 것으로 기대된다. 이번 연구는 Allen Foundation Inc., 한국연구재단 개인기초연구사업, 연세미래선도연구사업의 지원을 받아 수행됐다.